Der er nu kommet endnu et monoklonalt antistof rettet mod Amyloid-beta i hjernen, der beskrives som et “turning point” i behandlingen af Alzheimers Demens.
På Alzheimer’s Association International Conference 2023 (AAIC23) i Amsterdam blev et fase 3 studie for endnu et monoklonalt antistof rettet mod Amyloid-beta i hjernen præsenteret. Der findes allerede de to lægemidler Aducanumab og Lecanemab, der er godkendte i USA, men endnu ikke i EU. Denne gang var det så Eli Lilly and Company der kunne præsentere deres kandidat til de mulig fremtidige demenslægemidler. Dette skete på baggrund af TRAILBLAZER-ALZ 2 studiet, der blev publiceret i JAMA.
Sådan virker Donanemab
Donanemab er et monoklonalt antistof ligesom Aducanumab og Lecanemab rettet mod Amyloid-beta i hjernen. Amyloid-beta er en af de type aflejringer der ses i hjernen ved Alzheimers demens, hvor der senere i forløbet også kommer tau proteiner. Aflejringen af disse proteiner menes at være vigtig for udviklingen af Alzheimers Demens, og tanken er derfor at man ved at fjerne disse aflejringer kan fjerne eller forsinke sygdommen. Dette kaldes for Amyloid-kaskadehypotesen.
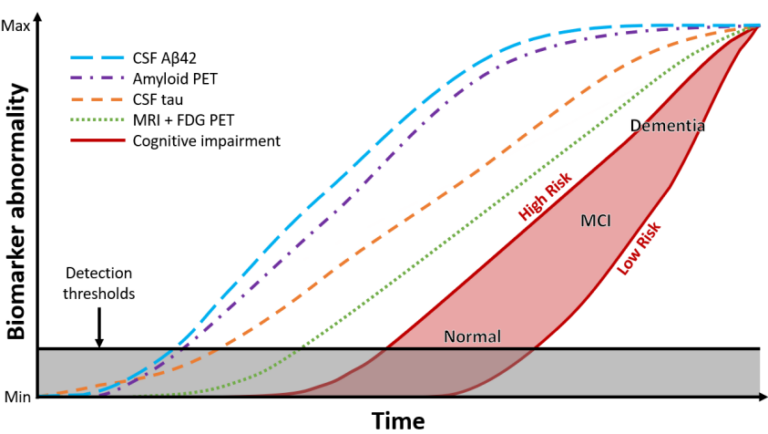
Der findes forskellige stadier af Amyloid-aflejringerne, og Donanemab er målrettet Amyloid-plaque – en af de sene stadier. Donanemab er kun rettet mod Amyloid-aflejringer, ikke tau proteiner. Når de monoklonale antistoffer binder til amyloid-beta i hjernen, fjernes disse fra hjernen. Man kan påvise amyloid og tau i hjernen enten ved en PET-scanning eller lumbalpunktur, og mængden af begge proteiner kan vurderes ved en PET-scanning. Eli Lilly producerer selv nogle af de PET essays der kan bruges til disse scanninger.
Af studiet fremgår tydeligt at Donanemab virker godt til at fjerne Amyloid-beta i hjernen. Allerede inden for 24 uger var stort set alt Amyloid fjernet.
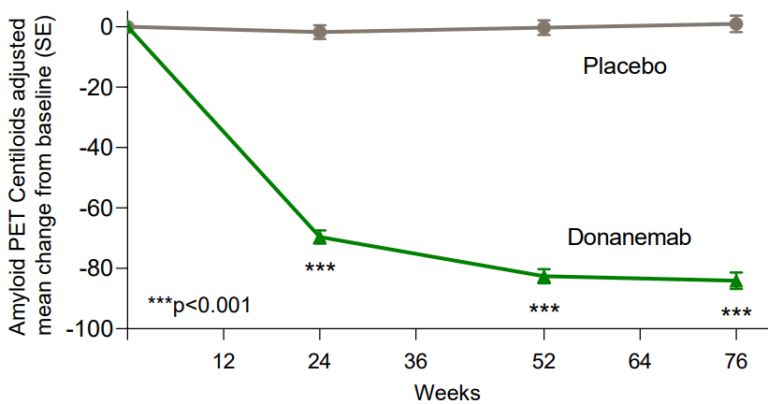
Der er altså ingen tvivl om at Donanemab virker fint ift. at fjerne Amyloid-beta i hjernen. Spørgsmålet er bare om dette også virker mod Alzheimers demens, ikke mindst den kognitive svækkelse der langsomt kommer med sygdommen.
Selve studiet
Studiet er et RCT studie, hvor halvdelen fik Donanemab og halvdelen fik placebo. Man fulgte deltagerne i 72 uger, altså ca. 1,5 år. Det primære endepunkt var iADRS skalaen, der er en skala for kognitiv svækkelse og funktionsnedsættelse der går fra 0 til 144 point, og hvor få point indikerer mere kognitiv svækkelse. I studiet så man at både dem der fik lægemidlet og dem der fik placebo langsomt fik mere kognitiv svækkelse, dvs. et fald på iADRS skalaen. Men dem der fik Donanemab gik det lidt langsommere. Efter 72 uger kunne man konstatere at dem der havde fået lægemidlet havde 3 point mere på iADRS skalaen sammenlignet med dem der havde fået placebo. Det er en absolut effekt på ca. 2%, men en relativ effekt på ca. 32%.
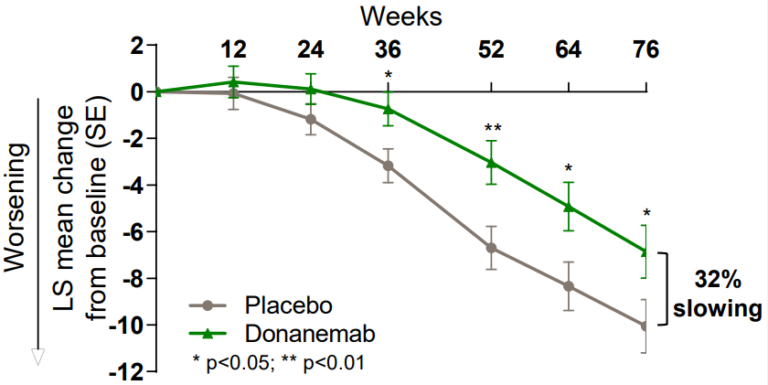
Som sekundært endepunkt blev der også kigget på CDR-SB skalaen – en skala fra 0 til 18, hvor en høj værdi indikerer mere kognitiv svækkelse. Denne skala er interessant fordi det er den skala der blev anvendt ved Aducanumab og Lecanemab. Her så man efter 72 uger en forskel i stigningen i point på 0,7.
Der var altså også en effekt på kognitiv svækkelse. Desværre ikke så tilstanden blev fjernet, altså ingen kur, men den tiltagende kognitive svækkelse gik lidt langsommere. Men spørgsmålet er om 3 point på en 144-pointskala er tilstrækkelig, og specielt om det er klinisk relevant. For at vurdere om en ændring er klinisk meningsfuld, har forskerne selv defineret det som at det var en ændring på mindst 20%, som blev opfyldt. Så forskerne mener selv det er en tilstrækkelig effekt som er klinisk meningsfuld. Ændringen i CDR-SB skalaen var som sagt kun 0,7 point, og her har andre studier estimeret et behov for en ændring på mindst 1-2 point for at det er klinisk meningsfuldt, og dette opfyldes ikke.
ARIA bivirkninger
Som de andre to monoklonale antistoffer var ARIA også en bivirkning ved Donanemab. ARIA er e billeddiagnostisk fænomen der er set ved behandling med anti-amyloide lægemidler, hvor man på en MRC ser tegn til mikroblødninger eller ødemer. Dette så man ved omkring 1 ud af 4 pt. der blev behandlet med Donanemab, og ud af dem havde 1 ud af 4 symptomer. Ja, faktisk var der under studiet 3 dødsfald, som man tilskrev ARIA.
I de fleste tilfælde er ARIA uden symptomer og forbigående. Men ARIA er et fænomen der er forholdsvis nyt, og som vi endnu ikke helt forstår. Vi ved ikke hvem der får det og hvordan det bedst behandles. Grunden så mange får ARIA vil behandlingen med lægemidlerne formentlig kræve at pt. bliver fulgt med MR scanninger.
Praktiske udfordringer
Hvis de nye lægemidler bliver godkendt i EMA, hvilket ingen indtil videre er blevet, så skal bl.a. Danmark tage stilling til om lægemidlet skal bruges. En af udfordringerne bliver prisen. Vi kender endnu ikke prisen for Donanemab, men prisen for Lecanemab blev estimeret til 180.000 kroner pr. person pr. år for behandling af lægemidlet.
Lægemidlet skal gives som en infusion hver 4. uge, hvilket er færre gange end Lecanemab der skal gives hver 2. uge. Det er vigtigt at for dem der skal behandles med lægemidlet skal man så regne med at de skal ind på sygehuset hver 4. uge, for at få deres infusion. Herudover skal de under behandlingen kontrolleres med bl.a. MR-scanninger grundet ARIA bivirkningen.
Der er også udfordringen ved selve udredningen. Ikke alle der får stillet diagnosen Alzheimers Demens får nemlig nødvendigvis foretaget en lumbalpunktur eller en PET-scanning og dermed påvist Amyloid og Tau, og dette vil være en forudsætning for behandling med lægemidlet. Lægemidlet henvender sig også til dem i det tidlige stadie, inklusiv dem med mild kognitiv impairment, hvilket er en større gruppe der i dag ikke behandles. Der skal altså tilføres en del ressourcer for at dette bliver nødvendigt, hvis lægemidlet skal indføres.
Lidt bedre end Lecanemab
Donanemab er marginalt bedre end Lecanemab. På CDR-SB skalaen så man en forskel på 0,7 point, hvor man ved Lecanemab så en forskel på 0,45 point. Den forskel vil dog formentlig ikke gøre nogen klinisk forskel.
Men ellers er der de praktiske ting at Donanemab kun skal gives som en infusion hver 4. uge, hvor Lecanemab skal gives hver 2. uge. Herudover er der ved Donanemab også forsøgt seponering af lægemidlet, så det ikke er livsvarigt. Det gjorde man ved at man stoppede med at give lægemidlet, når man på PET-scanninger kunne se at Amyloid var clearet tilstrækkeligt i hjernen.
Samlet set er Donanemab et formentlig dyrt lægemiddel med kun beskeden effekt og stor risiko for en alvorlig bivirkning. Det vil formentlig blive godkendt i USA, men det er usikkert om EMA også vil godkende det. Hvis det sker skal der i Danmark være en politisk diskussion om lægemiddlets effekt står mål med den høje omkostning og de svære bivirkninger.
Referencer
- Slides fra AAIC23 præsentationen.
- Sims JR, Zimmer JA, Evans CD, et al. Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA. Published online July 17, 2023. doi:10.1001/jama.2023.13239
- Manly JJ, Deters KD. Donanemab for Alzheimer Disease—Who Benefits and Who Is Harmed? JAMA. Published online July 17, 2023. doi:10.1001/jama.2023.11704
- Rabinovici GD, La Joie R. Amyloid-Targeting Monoclonal Antibodies for Alzheimer Disease. JAMA. Published online July 17, 2023. doi:10.1001/jama.2023.11703
- Widera EW, Brangman SA, Chin NA. Ushering in a New Era of Alzheimer Disease Therapy. JAMA. Published online July 17, 2023. doi:10.1001/jama.2023.11701