Antibiotika er lægemidler der anvendes til behandling af bakterielle infektioner. Denne artikel vedrører generelle forhold omkring antibiotika. Læs mere om de enkelte former for antibiotika.
Empirisk antibiotika ved ukendt ætiologi
Her kommer eksempler på antibiotikavalg og dosisforslag ved forskellige infektioner, hvor man har et formodet fokus, men ikke kender ætiologi. Det er vigtigt at orientere sig i lokale guidelines for dette, da anbefalinger her kan variere. Kilderne til denne artikel er de regionale antibiotikaguidelines og der er angivet hvilken guideline det stammer fra. Der angives her empirisk behandling, ved påvist agens skal målrettes behandling efter dette.
Appendicit
Ved ukompliceret appendicit er førstevalg Ampigenta kombineret med Metronidazol.
- Ampicillin 2 g i.v + Gentamicin 5-7 mg/kg i.v + Metronidazol 1 g i.v.
- Ved penicillinallergi: Gentamicin 5-7 mg/kg i.v + Metronidazol 1 g i.v.
Ved kompliceret appendicit er førstevalg Tazocin.
- Tazocin 4 g/0,5 g i.v. x 3
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser
Clostridioides difficile infektion
Førstevalg ved Clostridioides difficile infektion er Vancomycin. Ved fulminant C. difficile infektion vil man tillægge Metronidazol 500 mg i.v. x 2-3. Fidaxomicin er andetvalg i svære tilfælde, hvor Metronidazol er andetvalg i lette tilfælde. Man bør overveje FMT.
- Vancomycin 125 mg p.o. x 4 i 10 dage
Conjunctivitis
Ved bakterielt conjunctivitis er Kloramfenikol førstevalg.
- Kloramfenikol 1 dr. x 6 dgl. i maks. 10-14 dage.
Divertikulitis
Ukompliceret divertikulitis behandles som regel ikke med antibiotika. Ved kompliceret divertikulitis er førstevalg Tazocin. Ved sepsis og penicillinallergi suppleres Cefuroxim med Gentamicin.
- Tazocin 4 g/0,5 g i.v. x 3
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser
Epiglottitis acuta
Ved epiglottitis acuta er førstevalg Ceftriaxon.
- Ceftriaxon 2 g i.v. x 1 i 5 dage
Erysipelas
Ved erysipelas er førstevalg penicillin. Ved inficerede sår eller behandlingssvigt kan man dog supplere med enten Dicloxacillin eller Cloxacillin 1 g i.v/p.o. x 4.
- Benzylpenicillin 1,2 g (2 MIE) i.v. x 4 / Phenoxymethylpenicillin 0,6-0,8 g (1-1,2 MIE) p.o. x 4 i 5 dage
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 / Roxithromycin 300 mg p.o. x 1 i 5 dage
Erythema migrans
Ved erythema migrans (borrelia) er førstevalg penicillin.
- Phenoxymethylpenicillin 990 mg (1,5 mill. IE) p.o. x 3 i 10 dage
- Ved penicillinallergi: Doxycyclin 100 mg p.o. x 2 i 10 dage
Gastroenteritis
Ved gastroenteritis er antibiotika som regel ikke indiceret. Ved medtaget almentilstand, høj alder eller immunosupprimerede patienter er førstevalg dog Ciprofloxacin eller Azithromycin. Hvis gastroenteritis er erhvervet i udlandet, ses der ofte resistens overfor Ciprofloxacin. Ved sepsis på baggrund af gastroenterit vil man ofte vælge Ceftriaxon.
- Ingen antibiotika
- I nogle tilfælde: Ciprofloxacin 500 mg p.o. x 2 i 5 dage /Azithomycin 500 mg p.o. x 1 i 3 dage
Impetigo
Ved impetigo er førstevalg fjernelse af sårskorper, vask med klorhexidinsæbe og smøre med Klorhexidincreme. Kun ved udbredte læsioner eller bulløs impetigo er der indikation for antibiotika, hvor førstevalg er Dicloxacillin. Ved behandlingssvigt med Klorhexidin kan man i nogle tilfælde forsøge fusidincreme, men anvendelsen af dette skal begrænses grundet resistensudvikling.
- Klorhexidinsæbe 4% + Klorhexidincreme 1%
- Dicloxacillin 1 g p.o. x 4 i 7 dage ved udbredte læsioner eller bulløs impetigo
- Ved penicillinallergi: Roxithromycin 150 mg p.o. x 2 i 7 dage.
Infektion med ukendt fokus
Ved ukendt fokus, vil man ofte vente med opstart af antibiotika til svar på undersøgelser og gennemdyrkning, såfremt pt. er stabil. Såfremt fokus ikke findes vil førstevalg til antibiotika-behandling ofte være ampigenta, evt. kombineret med Metronidazol ved mistanke til abdominalt fokus. Ved kontraindikation til Gentamicin vil man vælge Tazocin.
- Ampicillin 2 g x 4 i.v. + Gentamicin 5 mg/kg i.v. + evt. Metronidazol 1g x 1 i.v./p.o.
- Cefuroxim 750 mg x 4 + Ciprofloxacin 500 mg x 2 p.o./400 mg x 2 i.v. + evt. Metronidazol 1g x 1 i.v./p.o.
KOL i exa
Ved KOL i exa er førstevalg Amoxicillin eller Benzylpenicillin i nogle regioner, mens det i andre regioner er Bioclavid. Ved manglende effekt inden for 48 timer kan man skifte til hhv. Bioclavid og Tazocin.
- Amoxicillin 1 g p.o. x 3 / Benzylpenicillin 1,2 g (2 MIE) i.v. x 4 i 5 dage
- Ved penicillinallergi: Doxycyclin 100 mg p.o. x 2 første døgn efterfulgt af 100 mg p.o. x 1 / Cefuroxim 1,5 g i.v. x 3 i 5 dage
Kolecystit/Kolangit
Ved mild ukompliceret kolecystit er førstevalg Ampicillin kombineret med gentamicin og metronidazol.
- Ampicillin 2 g i.v. + Gentamicin 5-7 mg/kg i.v. + Metronidazol 1 g i.v.
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. + Metronidazol 1 g i.v.
Ved moderat eller kompliceret kolecystit er førstevalg Tazocin.
- Tazocin 4 g/0,5 g i.v. x 3
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser
Ved svær eller kompliceret kolecystit er førstevalg Tazocin.
- Tazocin 4 g/0,5 g i.v. x 3
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Gentamicin 5-7 mg/kg i.v. x 1 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser
Ved kolangfit er førstevalg Tazocin.
- Tazocin 4 g/0,5 g i.v. x 3
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser + Gentamicin ved sepsis
Meningitis
Ved meningitis er førstevalg Ceftriaxon og Benzylpenicillin. Anbefaling af dosis og dosishyppighed for penicillin kan variere fra region til region. Desuden gives Dexametason 10 mg i.v. x 4 (0,15 mg/kg i.v. x 4) inden for 4 timer efter opstart af antibiotika og evt. Aciclovir 10 mg/kg x 3 i.v..
- Ceftriaxon 4 g i.v. x 1 + benzylpenicillin 1,8 g (3 MIE) i.v. x 6
- Ved penicillinallergi: Meropenem 2 g i.v. x 3
Nekrotiserende fasciitis
Ved nekrotiserende fasciitis er førstevalg Meropenem kombineret med Clindamycin. Dog kan anbefalingen variere fra region til region.
- Meropenem 2 g i.v. initialt, derefter 2 g x 3 i.v. + Clindamycin 600 mg x 3 i.v.
Osteomyelitis
Ved osteomyelitis er førstevalg Cloxacillin.
- Cloxacillin 1 g i.v. x 4
Otitis media
Ved Otitis media er førstevalg penicillin.
- Phenoxymethylpenicillin 0,6-0,8 g (1-1,2 MIE) p.o. x 3 i 5 dage
- Ved penicillinallergi: Roxithromycin 300 mg p.o. x 1
Perforeret hulorgan
Ved samfundserhvervet perforeret hulorgan med lav risiko er førstevalg Tazocin.
- Tazocin 4 g/0,5 g i.v. x 3
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser
Ved samfundserhvervet perforeret hulorgan i nedre GI-kanal med høj risiko tillægges Metronidazol.
- Tazocin 4 g/0,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Gentamicin 5-7 mg/kg i.v. x 1 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser
Ved samfundserhvervet perforeret hulorgan i øvre GI-kanal med høj risiko vil man også tillægge Fluconazol.
- Tazocin 4 g/0,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser + Fluconazol 400 mg i.v. x 1 (første dosis 800 mg)
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Gentamicin 5-7 mg/kg i.v. x 1 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser + Fluconazol 400 mg i.v. x 1 (første dosis 800 mg)
Ved hospitalserhvervet perforeret hulorgan kombineres følgende. Hvis pt. er behandlet med Fluconazol op til, anvendes i stedet caspofungin eller anidulafungin. Ved hospitalserhvervet perforeret hulorgan og sepsis, organsvigt eller indlæggelse på intensiv anvendes i stedet Meropenem og Fluconazol.
- Tazocin 4/0,5 g i.v. x 3 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser + Fluconazol 400 mg i.v. x 1 (første dosis 800 mg)
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + Gentamicin 5-7 mg/kg i.v. x 1 + Metronidazol 1-2 g dgl. fordelt på 2-3 doser + Fluconazol 400 mg i.v. x 1 (første dosis 800 mg)
Pneumoni
Ved let samfundserhvervet pneumoni er førstevalg Benzylpenicillin eller Phenoxymethylpenicillin. Dosis kan variere i anbefalingen fra forskellige regioner.
- Benzylpenicillin 1,2 g (2 MIE) i.v. x 4 / Phenoxymethylpenicillin 0,6-0,8 g (1-1,2 MIE) p.o. x 4 i 5 dage
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 / Roxithromycin 300 mg p.o. x 1 i 5 dage
Ved moderat-svær samfundserhvervet pneumoni er førstevalg Benzylpenicillin suppleret med engangsdosis Azithromycin. Azithromycin forlænges ved påvist atypisk agens. I nogle regioner anvendes Clarithromycin i stedet for Azithromycin, men Clarithromycin er associeret med flere interaktioner, højere kardiotoksicitet og mulig større effekt ved legionellapneumoni.
- Benzylpenicillin 1,2 g (2 MIE) i.v. x 4 i 7 dage + EO azithromycin 500 mg i.v
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 i 7 dage + EO azithromycin 500 mg i.v.
Ved svær samfundserhvervet pneumoni er førstevalg Tazocin suppleret med Azithromycin. I nogle regioner anbefales dog Cefuroxim i lavdosis i stedet for Tazocin.
- Tazocin 4 g/0,5 g i.v. x 3 i 7 dage + EO azithromycin 500 mg i.v
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 i 7 dage + EO azithromycin 500 mg i.v.
Ved sygehuserhvervet pneumoni er førstevalg Tazocin. I nogle regioner anvender man dog i.v. Bioclavid i stedet.
- Tazocin 4 g/0,5 g i.v. x 3 i 7 dage
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 i 7 dage
Ved aspirationspneumoni er førstevalg det samme som normalt for pneumoni. Dog vil man ved sygehuserhvervet pneumoni og penicillinallergi supplere Cefuroxim med Metronidazol. I nogle regioner anbefaler man dog at vælge Tazocin eller Bioclavid i stedet for penicillin.
Ved KOL og pneumoni er behandlingen den samme som normal pneumoni. I nogle regioner anbefaler man dog at vælge bioclavid fremfor penicillin.
Sepsis
Førstevalg ved sepsis er ampigenta. Gentamicin gives i maksimalt 3 døgn med maksimal dosis på 500 mg pr. døgn. Hvis gentamicin ikke kan gives, anvendes Tazocin i stedet. Ved mistanke til intraabdominalt fokus tillægges Metronidazol, dog ikke ved Tazocin eller Meropenem. I nogle regioner er Tazocin kombineret med gentamicin førstevalg fremfor ampigenta, men generelt er dækningsgraden af ampigenta større end tazocin og der ses stigende resistens af Tazocin.
- Ampicillin 2 g i.v. x 4 + gentamicin 5-7 mg/kg i.v. x 1
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 + gentamicin 5-7 mg/kg i.v. x 1
Ved septisk shock er førstevalg i stedet Tazocin, hvor man evt. kan supplere med gentamicin.
- Tazocin 4 g/0,5 g i.v. x 4 + evt. gentamicin 5-7 mg/kg i.v. x 1
- Ved penicillinallergi: Meropenem 1 g i.v. x 3
Septisk artrit
Ved septisk artrit er førstevalg benzylpenicillin suppleret med cloxacillin.
- Benzylpenicillin 1,2 g (2 MIE) i.v. x 4 + cloxacillin 1 g i.v. x 4
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3
Sinuitis
Ved kompliceret sinuitis er førstevalg penicillin. Ved ukompliceret sinuitis er der ikke effekt af antibiotika.
- Phenoxymethylpenicillin 0,6-0,8 g (1-1,2 MIE) p.o. x 3 i 7 dage
- Ved penicillinallergi: Roxithromycin 300 mg p.o. x 1 i 7 dage
Tonsilitis
Ved tonsilitis er førstevalg penicillin.
- Phenoxymethylpenicillin 0,6-0,8 g (1-1,2 MIE) p.o. x 3 i 7 dage
- Ved penicillinallergi: Roxithromycin 300 mg p.o. x 1 i 7 dage
UVI
Ved akut ukompliceret cystitis er førstevalg Nitrofurantoin, Pivmecillinam eller Trimethoprim.
- Nitrofurantoin 50 – 100 mg p.o. x 4 / Pivmecillinam 400 mg p.o. x 3 / Trimethoprim 200 mg p.o. x 2 i 3 dage
- Ved penicillinallergi: Nitrofurantoin 50 – 100 mg p.o. x 4 / Trimethoprim 200 mg p.o. x 2 i 3 dage
Ved kompliceret ikke-indlæggelseskrævende cystitis er førstevalg Pivmecillinam.
- Pivmecillinam 400 mg p.o. x 3 i 5 dage
- Ved penicillinallergi: Trimethoprim 200 mg p.o. x 2 i 5 dage ved upåvirket almen tilstand og afebril eller Ciprofloxacin 500 mg p.o. x 2 i 5 dage ved påvirket almen tilstand eller feber.
Ved akut ikke-indlæggelseskrævende pyelonefrit er førstevalg Pivmecillinam.
- Pivmecillinam 400 mg p.o. x 3 i 7 dage
- Ved penicillinallergi: Ciprofloxacin 500 mg p.o. x 2 i 7 dage
Ved akut indlæggelseskrævende kompliceret UVI er førstevalg Ampigenta. Hvis gentamicin ikke kan anvendes, vælges i stedet Tazocin. I nogle regioner anvendes dog Cefuroxim i lavdosis i stedet for Ampicillin.
- Ampicillin 2 g i.v. x 4 i 7 dage + Gentamicin 5-7 mg/kg i.v. x 1 i maks. 3 dage
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 i 7 dage + Gentamicin 5-7 mg/kg i.v. x 1 i maks. 3 dage
Ved urobakteriæmi er førstevalg enten ampigenta eller tazocin.
- Ampicillin 2 g i.v. x 4 i 7 dage + Gentamicin 5-7 mg/kg i.v. x 1 i maks. 3 dage / Tazocin 4/0,5 g i.v. x 3 i 7 dage
- Ved penicillinallergi: Cefuroxim 1,5 g i.v. x 3 i 7 dage + Gentamicin 5-7 mg/kg i.v. x 1 i maks. 3 dage
Empirisk antibiotika ved kendt ætiologi, men ukendt resistens
Her kommer eksempler på antibiotikavalg ved kendt ætiologi, men hvor der endnu ikke foreligger resistenssvar. Når der foreligger resistenssvar skal behandlingen rettes mod dette. Foreslagene er angivet som førstevalg, ved ikke penicillinallergi.
| Bakterie | Muligt antibiotikavalg | Bemærkning |
|---|---|---|
| Chlamydia pneumoniae | Azithromycin / Roxithromycin | |
| Chlamydia psittaci | Azithromycin / Roxithromycin | |
| E. coli | Tazocin / Bioclavid | Hvis e. coli er følsom for Ampicillin kan det anvendes, men ca. 40% er resistente |
| Enterococcus faecalis | Ampicillin / Amoxicillin | |
| H. influenzae | Tazocin / Bioclavid | Hvis H. influenzae er ampicillinfølsom er Ampicillin førstevalg |
| Hæmolytiske streptokokker | Benzylpenicillin / Phenoxymethylpenicillin | |
| Klebsiella pneumoniae | Tazocin / Pivmecillinam | Klebsiella er naturlig resistent overfor Ampicillin |
| Legionella pneumophila | Azithromycin | |
| Listeria monocytogenes | Ampigenta | |
| Meningokokker | Benzylpenicillin | |
| Moraxella catarrhalis | Tazocin / Bioclavid | |
| Mycoplasma pneumoniae | Azithromycin / Roxithromycin | |
| Pneumokokker | Benzylpenicillin / Phenoxymethylpenicillin | |
| Pseudomonas aeruginosa | Tazocin / Ciprofloxacin | |
| Proteus mirabilis | Nitrofurantoin / Amoxicillin / Pivmecillinam / Trimethoprim / Sulfamethizol | |
| S. aureus | Cloxacillin / Dicloxacillin | Hvis penicillinfølsom er penicillin førstevalg. S. aureus er ofte kolonisation i luftveje. |
| S. saprophyticus | Nitrofurantoin / Dicloxacillin / Trimethoprim / Sulfamethizol |
Antibiotikaspektrum
Et antibiotikaspektrum angiver hvilke antibiotika visse bakterier typisk er følsom overfor. Dette kan blandt andet anvendes ved valg af antibiotika til empirisk behandling. Nedenunder ses et eksempel på dette, hvor de antibiotika der er angivet med rødt er antibiotika hvor forbruget generelt skal begrænses.

Dosering overvægt
Ved overvægt (vægt>120 kg) vil man ofte anvende en højere dosis eller øget dosishyppighed:
- Benzylpenicillin 1,8 g (3 MIE) i.v. x 4
- Cloxacillin 2 g i.v. x 4
- Cefuroxim 1,5 g i.v. x 4
- Tazocin 4/0,5 g i.v. x 4
- Meropenem 2 g i.v. x 3
- Ciprofloxacin 500-750 mg p.o x 2 / 500mg p.o x 3 / 600 mg i.v. x 2
- Metronidazol anvendes uden at ændre dosering
Dosering nyresvigt
Her angives eGFR grænser hvor man skal overveje dosisreduktion.
| Normal dosis | eGFR 10-30 | eGFR<10 | |
|---|---|---|---|
| Amoxicillin | 1 g x 3 | 1 g x 2 | 1 g x 1 |
| Ampicillin | 2 g x 4 | 2 g x 3 | 2 g x 2 |
| Benzylpenicillin | 1,2 g x 4 | 1,2 g x 4 | 1,2 g x 4 |
| Bioclavid | 500/125 mg x 3 | 500/125 mg x 2 | 500/125 mg x 1 |
| Cefuroxim | 1,5 g x 3 | 1,5 g x 2 | 1,5 g x 1 |
| Ciprofloxacin | 500 mg x 2 | 500 mg x 1 | 500 mg x 1 |
| Cloxacillin | 1 g x 4 | 1 g x 4 | 1 g x 4 |
| Dicloxacillin | 1 g x 4 | 1 g x 4 | 1 g x 4 |
| Meropenem | 1 g x 3 | 1 g x 2 | 0,5 g x 1 |
| Phenoxymethylpenicillin | 1 MIE x 4 | 1 MIE x 4 | 1 MIE x 3 |
| Pivmecillinam | 400 mg x 3 | 400 mg x 3 | 400 mg x 2 |
| Tazocin | 4/0,5 g x 3 | 4/0,5 g x 2 (ved eGFR<20) | 4/0,5 g x 2 |
Dosering kontinuerlig behandling
Kontinuerlig antibiotikabehandling kan både lette håndteringen af behandlingen (antibiotika skal hænges op færre gange) og man kan optimere tiden over MIC, så behandlingen bliver mere effektiv overfor bakterier med en højere MIC (fx. Pseudomonas aeruginosa). Man kan fx. anvende mekaniske pumper (fx. CADD-pumper) eller elastomerpumper (fx. Easypump).
En del antibiotika der gives kontinuerligt skal grundet holdbarhed gives som kold infusion. Det betyder man skal anvende køletasker, der sikrer at temperaturen er 2-8 °C under infusionen. Man skal derfor orientere sig om holdbarhed inden anvendelse af antibiotika.
Kontinuerlig behandling fungerer ved at man først giver en loading dosis og herefter opsætter en pumpe med kontinuerlig behandling. En loading dosis gives typisk over 30 minutter.
| Antibiotika | Loading dosis | Kontinuerlig dosis |
|---|---|---|
| Ampicillin | 2 g | 8 g/døgn |
| Benzylpenicillin | 1,2 g | 4,8 g/døgn |
| Cefuroxim | 1,5 g | 4,5 g/døgn |
| Cloxacillin | 1 g | 4 g/døgn |
| Meropenem | 1 g | 3 g/døgn |
| Tazocin | 4/0,5 g | 12/1,5 g/døgn |
Skift fra i.v. til p.o. antibiotika
Generelt kan man skifte fra i.v. antibiotika til p.o. antibiotika hvis pt. er klinisk stabil, temperatur<37,8 grader, puls<100, faldende leukocytter og pt. er i stand til at indtage peroral medicin.
Nedenunder ses en tabel med forslag til hvilke p.o. alternativer man kan overveje til i.v. antibiotika. Det er vigtigt at forholde sig til lokale instrukser ift. dette også, da disse kan variere.
| Fokus | I.v. antibiotika | P.o. antibiotika |
|---|---|---|
| Luftveje | Benzylpenicillin | Phenoxymethylpenicillin |
| Tazocin | Bioclavid | |
| Cefuroxim/Cefotaxim/Ceftriaxon | Bioclavid/Roxithromycin | |
| Urinveje | Ampicillin | Pivmecillinam |
| Tazocin | Pivmecillinam | |
| Cefuroxim/Cefotaxim/Ceftriaxon | Pivmecillinam/Trimethoprim/Ciprofloxacin | |
| Hud/bløddele | Cloxacillin | Dicloxacillin/Flucloxacillin |
| Benzylpenicillin | Phenoxymethylpenicillin | |
| Tazocin | Phenoxymethylpenicillin | |
| Cefuroxim/Cefotaxim/Ceftriaxon | Phenoxymethylpenicillin/Roxithromycin | |
| Abdominalt | Tazocin | Overvej stop antibiotika |
| Cefuroxim/Cefotaxim/Ceftriaxon | Overvej stop antibiotika | |
| Andet fokus | Ampicillin | Amoxicillin |
| Benzylpenicillin | Phenoxymethylpenicillin | |
| Cloxacillin | Dicloxacillin/Flucloxacillin | |
| Mecillinam | Pivmecillinam | |
| Clarithromycin | Roxithromycin | |
| Ciprofloxacin | Ciprofloxacin | |
| Moxifloxacin | Moxifloxacin | |
| Metronidazol | Metronidazol | |
| Tazocin | Bioclavid | |
| Meropenem | Konferer med mikrobiologer |
Det er en myte at det er farligt at skifte antibiotika fra i.v. til p.o. ved bakteriæmi og at i.v. antibiotika er bedre end p.o. antibiotika. Et systematisk review fra 2024 undersøgte om tidlig skift fra i.v. til oral antibiotika ved bakteriæmi og sepsis var lige så godt som sen skift. Man konkluderede her at 90 dages mortaliteten var ikke højere ved tidlig skift af antibiotika til p.o. sammenlignet med sen skift.
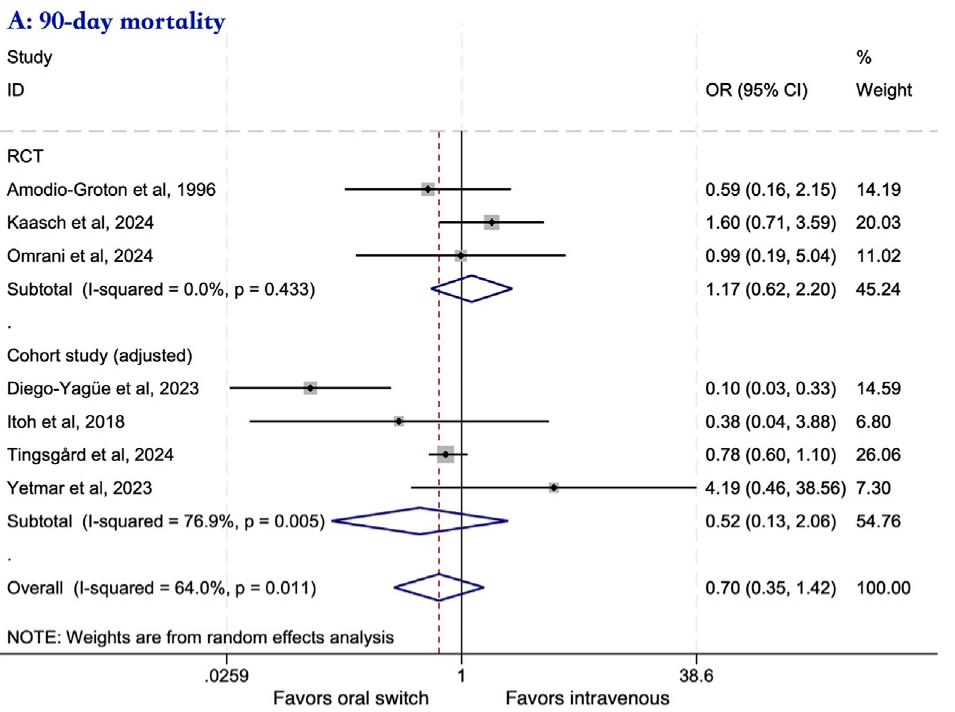
Et andet review fra 2025 hvor man undersøgte effekten af tidlig skift til p.o. antibiotika ved grampositive bakteriæmier støttede også tidlig skift til p.o. antibiotika ift. all-cause mortality.
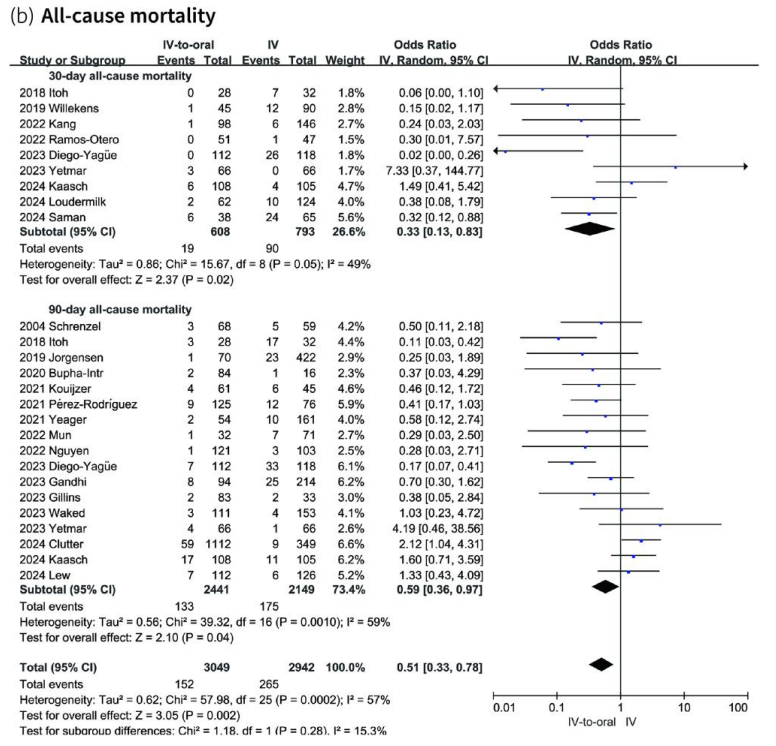
Effekt af antibiotika
Når man taler om effekten af antibiotika, skelnes der mellem forskellige typer af antibiotika:
- Tidsafhængig antibiotika
- Koncentrationsafhængig antibiotika
- Døgndosisafhængig antibiotika
For af forstå forskellen skal man se på Minimum Inhibitory Concentration (MIC), der er den koncentraton af et antibiotika i blodet som kræves for at det har effekt mod bakterier.
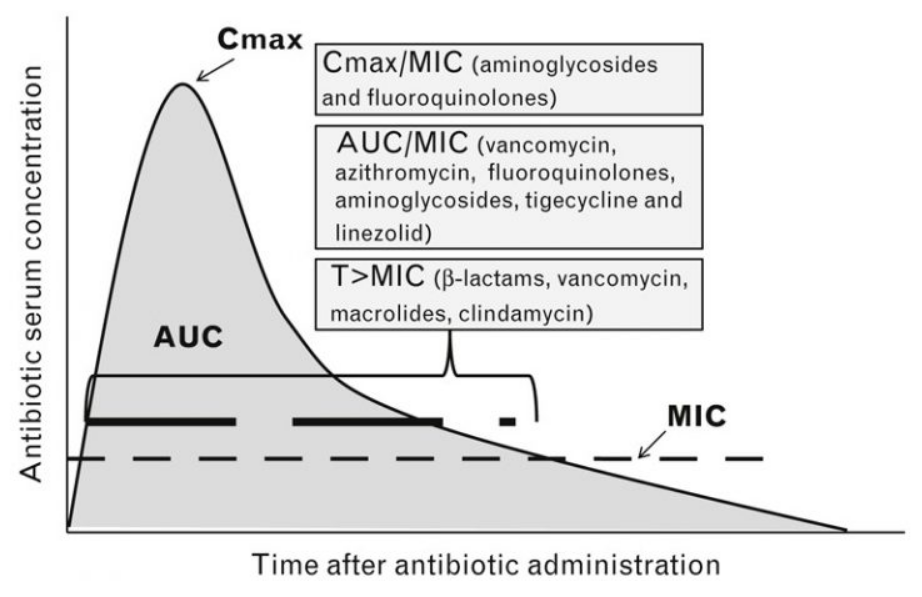
Tidsafhængig antibiotika er fx. betalaktam-antibiotika. Her fås ikke større effekt ved at øge dosis, men derimod ved hyppig dosering, således at tiden hvor den frie plasmakoncentation over MIC bliver så høj som mulig. Koncentrationen skal som tommelfingerregel være over MIC i mere end 50% af tiden. Makroliderne erythromycin, roxithromycin og clarithromycin er også tidsafhængig antibiotika.
Koncentrationsafhængig antibiotika er fx. aminoglykosider. Her skal man sikre sig at plasmakoncentrationen er over 8x MIC mindst én gang i døgnet, for at få en effekt. Makrolidet azithromycin er også koncentrationsafhængig.
Døgndosisafhængig antibiotika er hvor effekten afhænger af den samlede døgndosis og ikke ændrer sig ved at dele dosis op. Det er fx. fluoroquinoloner.
Ved effekten af antibiotika taler man også om penetransen, dvs. i hvor høj grad det enkelte antibiotikum formår at nå frem til infektionsstedet.
Desuden skelnes der mellem bakteriostatisk eller baktericid antibiotika. Bakteriostatisk antibiotika hæmmer vækst og formering af bakterier, men dræber dem ikke. Baktericide antibiotika er bakteriedræbende. Eksempler på bakteriostatisk antibiotika er makrolider og tetracykliner, mens eksempler på baktericide antibiotika er β-laktamer og Fluorokinoloner.
Antibiotikavarighed
Flere studier har vist at korte antibiotikakure er lige så godt som lange antibiotikakure. Derfor har man også forkortet antibiotikavarighed i guidelines de seneste år. Selvom infektionstal fortsat er høje, er dette formentlig et inflammatorisk respons der kommer efter bakterierne er bekæmpet. Kortere antibiotikakure er med færre bivirkninger og derfor bedre.
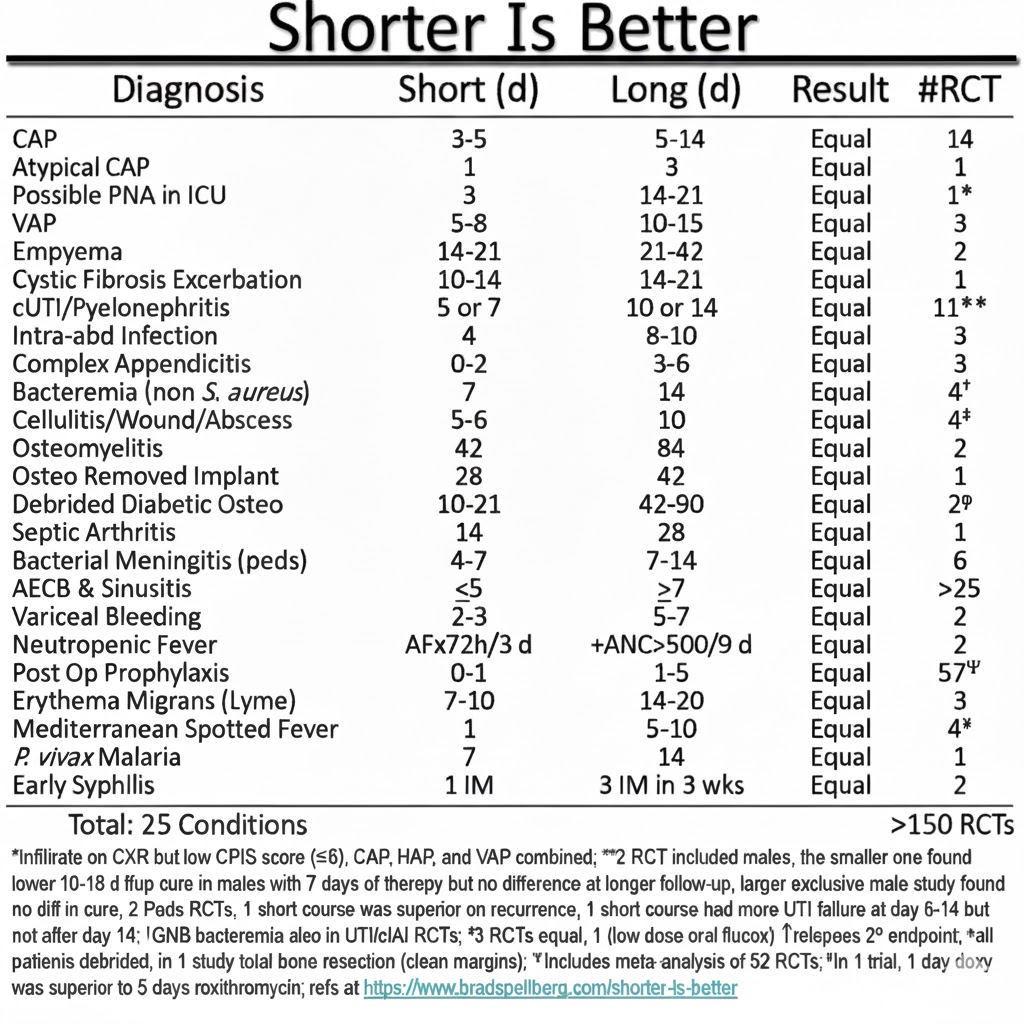
For nogle infektioner kan længere antibiotikabehandlinger være nødvendige, som fx. proteseinfektioner.
Antibiotikallergi
Ved penicillinallergi eller mistanke hertil, kan man ofte alligevel anvende cefalosporin, da der meget sjældent ses krydsallergi, undtagen hvis der er fælles sidekæder (som aminopenicilliner og cefalexin). Ved en akut situation er cefuroxim og 3. generations cefalosporiner (fx. ceftriaxon), da den terapeutiske gevinst ift. alternativer overstiger risikoen for anafylaksi.
Target for antibiotika
Antibiotika har forskellige targets på bakterier, og generelt kan man inddele i følgende kategorier:
- Cellevægssyntesehæmmere
- Proteinsyntesehæmmere
- Nukleinsyresyntesehæmmere
- Inhibering af folatsyntese
- Destruktion af cellemembran
Antibiotika der virker hæmning af cellevægssyntesen, virker ved at hæmme peptidoglycan syntesen eller krydsbinding af peptidoglycan. Beta-lactamer som Penicilliner og Cefalosporiner binder og inaktiverer penicillin-bindende proteiner (PBP), der er vigtig for peptidoglycan krydsbindingen i cellevæggen. Dette fører til en defekt cellevæg, der går i stykker og fører til at bakterien dræbes. Et andet eksempel er Glykopeptider som Vancomycin, der også hæmmer opbygningen af peptidoglycan.
Proteinsyntesehæmmere er målrettet ribosomer i bakterierne. Aminoglykosider som Gentamicin binder til ribosomerne, hvilket fører til en fejllæsning af mRNA og deraf defekte proteiner. Makrolider som Azithromycin binder også til ribosomer, og fører til at peptidkæderne ikke kan blive forlænget. Tetracykliner blokerer for tRNA’s adgang til ribosomet. Kloramfenikol og Linezolid er andre eksempler af denne klasse af antibiotika.
Nukleinsyresyntesehæmmere blokerer for bakteriernes evne til at replikere DNA eller transcribere det til RNA. Quinoloner og Fluoroquinoloner hæmmer fx. enzymer som DNA-gyrase og topoisomerase, der er nødvendige for at optwiste og pakke bakteriens DNA. Rifampicin hæmmer bakteriens RNA-polymerase og forhindrer dermed transskriptionen til mRNA.
Folatsyntesehæmmere virker ved hæmme enzymer i bakteriernes evne til at producere folinsyre. Dette er nødvendig for at bakterierne kan producere nukleotider. Sulfonamider og Trimethoprim er eksempler på denne type antibiotika. Anvendelse af begge antibiotika har en synergistisk effekt.
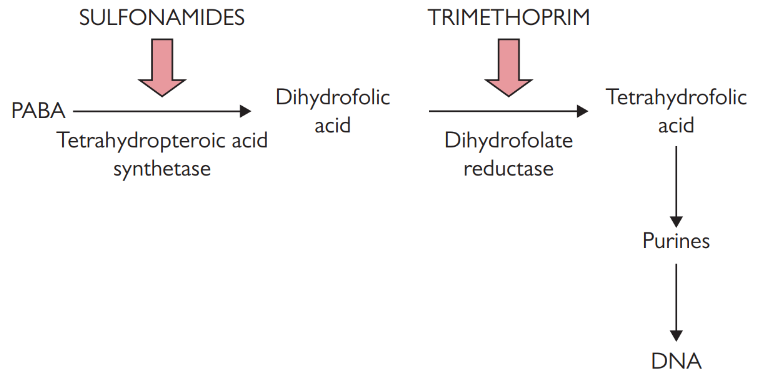
Antibiotika der virker ved destruktion af cellemembranen er fx. Polymyxiner (fx. Colistimethatnatrium).
Antibiotikaresistens
Antibiotikaresistens (AMR) er et samfundsproblem som det er vigtigt at være opmærksom på, da stigende antibiotikaresistens kan føre til flere infektioner det ikke er muligt at behandle. I Danmark har vi haft meget fokus på dette, og antibiotikaresistens er heller ikke så udbredt i Danmark som mange andre steder i verden. På verdensplan menes antibiotikaresistens at være skyld i 10 millioner dødsfald hvert år.
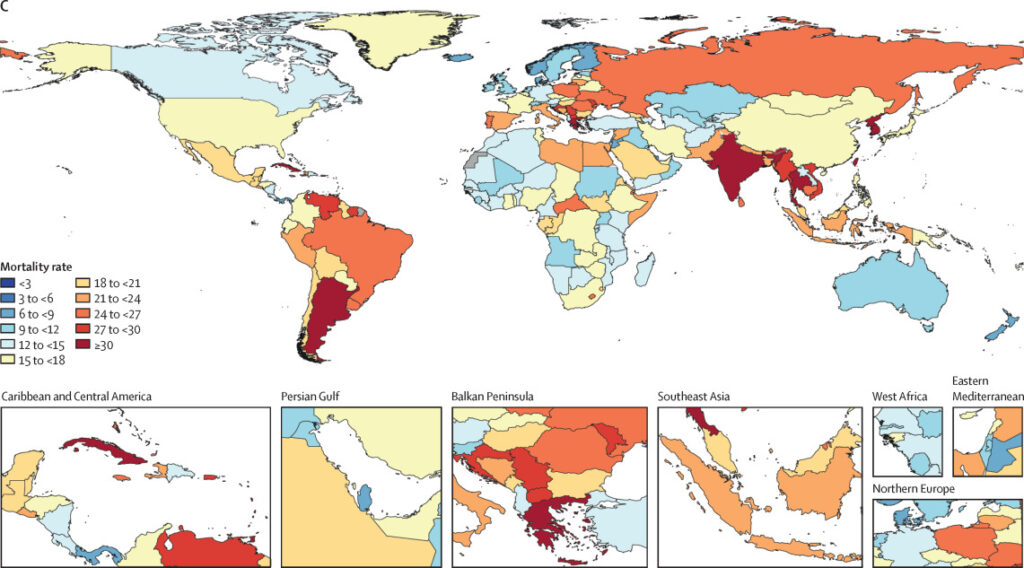
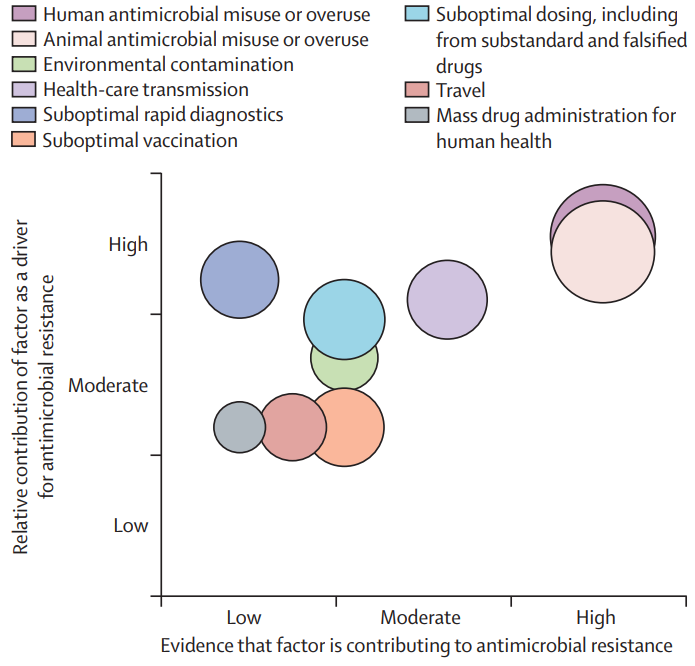
Det er især overforbruget af antibiotika hos dyr og mennesker der driver udviklingen af antibiotikaresistens. Det er netop derfor der er meget fokus i at nedbringe antibiotikaforbruget, specielt bredspekret antibiotika. Vacciner er også en vigtig faktorer, der menes at kunne nedbringe antibiotikaforbruget med 22% og mortaliteten ved antibiotikaresistens med 10%. Herudover er der faktorer som håndhygiejne, kateterhygiejne, penicillinallergi-udredning, vaginal østrogen, Methenamin, tranebær og at rense spildevand fra hospitaler.
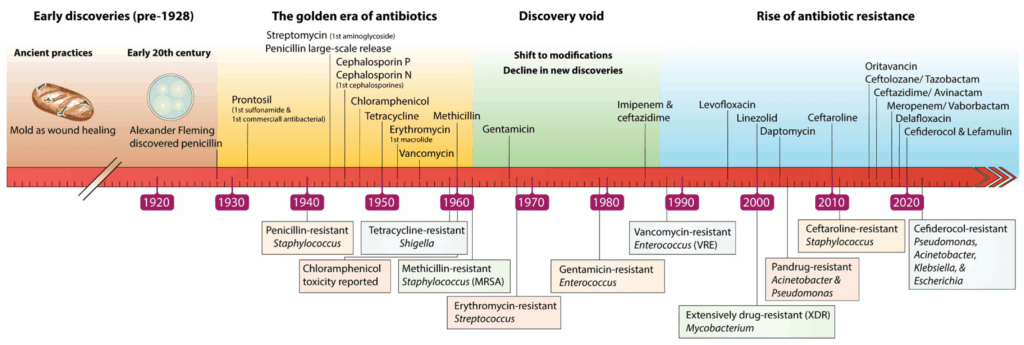
Når der udvikles ny antibiotika ses resistens mod dette nogle år efter. Gentamicin kom fx. i 1960øerne og i slutningen af 1970’erne kom resistens mod dette. Der er en tendens til at resistensen kommer hurtigere efter ny antibiotika i nyere tid. Der udvikles heller ikke så meget antibiotika som før i tiden.
AWARE-klassifikationen
AWARE-klassifikationen opdeler antibiotika i forhold til hvilke der er førstevalg, hvilke hvor forbruget skal begrænses og hvilke der må betragtes som sidste mulighed. Bemærk at Tazocin her er placeret i gul kategori, mens ampigenta er placeret i grøn kategori.

Resistensmekanismer
Der skelnes mellem naturlig resistens og erhvervet resistens. Et eksempel på naturlig resistens er mycoplasma der er naturligt resistente overfor antibiotika der angriber cellevæggen, fordi bakterien ikke har nogen cellevæg. Et andet eksempel er klebsiella, der har et gen der koder for enzymet SHV-1 β-laktamase, der nedbryder β-laktam-ringen i penicilliner som ampicillin, hvorfor klebsiella er naturligt resistente overfor ampicillin.
Erhvervet resistens er potentielt reversibelt, og skyldes at bakterier tilpasser sig et antibiotikamiljø. De hyppigste former for erhvervet resistens er:
- Targetændring
- Enzymatisk inaktivering
- Impermeabilitet
- Efflux-pumper
Ved targetændring er target for antibiotika ændret, så det ikke længere virker. Et eksempel er MRSA der erhverver sig et mecA gen, som koder for proteinet PBP2a i bakteriecellemembranen, der overtager opbygningen af cellevæggen fra de naturlige PBP, som penicilliner normalt angriber. Antibiotika har ikke samme affinitet for PBP2a som PBP, hvorfor bakterien fortsat kan opbygge en cellevæg og dermed virker antibiotika ikke.
Ved enzymatisk inaktivering udvikler bakterierne enzymer der klipper β-laktamringen over. Et eksempel er S. aureus der producerer Penicillinase som gør den resistent overfor penicillin. Et andet eksempel er ESBL (Extended Spectrum Beta-Lactamase), hvor fx. e. coli eller klebsiella producerer enzymer der kan nedbryde et bredt spektrum af β-laktamantibiotika. Dette gør dem resistente overfor penicilliner og 3. generations cefalosporiner, men enzymerne kan ofte hæmmes af β-Laktamase-hæmmere, hvorfor bioclavid og tazocin vil være effektive. Et andet eksempel er AmpC, der er et β-Laktamase-enzym der hydrolyserer β-Laktamringen hos specielt cefalosporiner og penicilliner.
Effluxpumper er en resistensmekanisme, hvor bakterier erhverver sig effluxpumper der kan genkende visse former for antibiotika, og pumpe dem ud før de virker. Et eksempel er pneumokokker, der via plasmider får mef(A) der er en makrolid effluxpumpe.
Ved impermeabilitet erhverver bakterierne resistens ved at gøre bakterierne impermeable overfor antibiotika. Et eksempel er tab af poriner, der er kanaler i bakteriernes ydre membran, som antibiotika kommer ind i bakterien ved. Ved at disse poriner enten ikke bliver produceret eller defekte, kan antibiotika ikke komme ind til deres target. Fx. ses ved Klebsiella pneumoniae tab af OmpK35/OmpK36 der giver nedsat følsomhed for carbopenemer.
Ved spredning af resistens spiller specielt plasmider en væsentlig rolle. Plasmider er cirkulære, dobbeltstrengede DNA-molekyler, som bakterierne kan sprede mellem hinanden og på den måde sprede resistensgener mellem bakterier, herunder også andre bakteriearter. Plasmider kan bære flere resistensgener på en gang.
Multiresistens
Multiresistente bakterier er bakterier der er resistente overfor flere klasser af antibiotika, hvilket gør dem sværere at behandle. Eksempler er MRSA, VRE, ESBL og CPO. ESBL producerende bakterier producerer enzymer der kan nedbryde et bredt spektrum af β-laktamantibiotika. CPO er en undergruppe af ESBL, der også har opnået resistens overfor antibiotika man normalt bruger til at behandle ESBL. MRSA er en form for stafylokokker, der gør dem resistente overfor penicilliner og cefalosporiner. VRE er enterokokker (fx. enterococcus faecium eller enterococcus faecalis) som er blevet resistente overfor Vancomycin.
Referencer
Her kan du finde en liste med referencer der er anvendt i denne artikel. Der er også angivet direkte henvisninger i teksten samt ved anvendelse af billeder og figurer.
- Strategi for sundhedssektorerhvervede infektioner og antibiotikaforbrug (Region Syd)
- Tidligt skift fra intravenøs til oral antibiotikabehandling (Ugeskrift for læger)
- Dosera klokt för bästa effekt – etablerade riktlinjer vägleder (Infektionsguiden)
- Effekt i relation til farmakokinetik og farmakodynamik (Promedicin)
- Breakpoint tables for interpretation of MICs and zone diameters
- Antibiotika – dosering, forholdsregler og behandlingsrekommandationer – håndbog (Riget)
- Antibiotikavejledning for primærsektoren (Region H)
- Nye retningslinjer for antibiotikadosering til patienter med nedsat nyrefunktion og patienter i hæmodialyse (Ugeskriftet)
- Global burden of bacterial antimicrobial resistance 1990–2021: a systematic analysis with forecasts to 2050Naghavi, Mohsen et al.The Lancet, Volume 404, Issue 10459, 1199 – 1226
- Holmes AH, Moore LS, Sundsfjord A, Steinbakk M, Regmi S, Karkey A, Guerin PJ, Piddock LJ. Understanding the mechanisms and drivers of antimicrobial resistance. Lancet. 2016 Jan 9;387(10014):176-87. doi: 10.1016/S0140-6736(15)00473-0. Epub 2015 Nov 18. PMID: 26603922.
- Tahmasebi H, Arjmand N, Monemi M, Babaeizad A, Alibabaei F, Alibabaei N, Bahar A, Oksenych V, Eslami M. From Cure to Crisis: Understanding the Evolution of Antibiotic-Resistant Bacteria in Human Microbiota. Biomolecules. 2025; 15(1):93. https://doi.org/10.3390/biom15010093
- Strategi for sundhedssektorerhvervede infektioner og antibiotikaforbrug (Region Syd)
- National handlingsplan for antimikrobiel resistens hos mennesker (Indenrigs- og sundhedsministeriet)
- Li Q, Zhou Q, Fan J, Huang S, Chen Y, Song F, Fu Z, Liu E, Tang D, Zeng L, Luo Z. Oral switch vs. continued intravenous antibiotic therapy in patients with bacteraemia and sepsis: a systematic review and meta-analysis. Clin Microbiol Infect. 2025 Apr;31(4):551-559. doi: 10.1016/j.cmi.2024.11.035. Epub 2024 Dec 4. PMID: 39643210.
- Tan Z, Liang W, Zhang N, Liang B, Bai N, Cai Y. Efficacy and safety of earlier switching to an oral antibiotic therapy for the treatment of Gram-positive bloodstream infections: a systematic review and meta-analysis. J Antimicrob Chemother. 2025 Sep 3;80(9):2344-2360. doi: 10.1093/jac/dkaf209. PMID: 40660856.
- Cefalosporiner (β-laktamantibiotika) (Promedicin)
- Antibiotikavejledning Region Syd
- Initial antibiotika behandling af udvalgte samfundserhvervede bakterielle infektioner hos voksne immunkompetente patienter, regional retningslinje (Region Midt)
Lignende lægemidler
Lægemidler i ATC-gruppen J01

Skriv et svar